Revefenacin
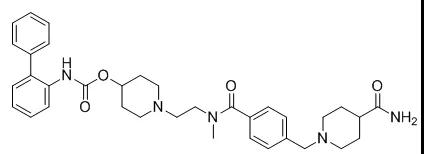
Revefenacin最初由Theravance Biopharma研发,2015年,Theravance Biopharma与Mylan达成一项共同研发该药对于治疗呼吸系统疾病的协议。该药于2018年11月9日获FDA批准上市,商品名为Yupelri®。Yupelri®是一种毒蕈碱型乙酰胆碱能受体(mAChRs)拮抗剂,获批用于治疗慢性阻塞性肺病(COPD)。推荐给药剂量为175 ug每次,每日一次[1]。
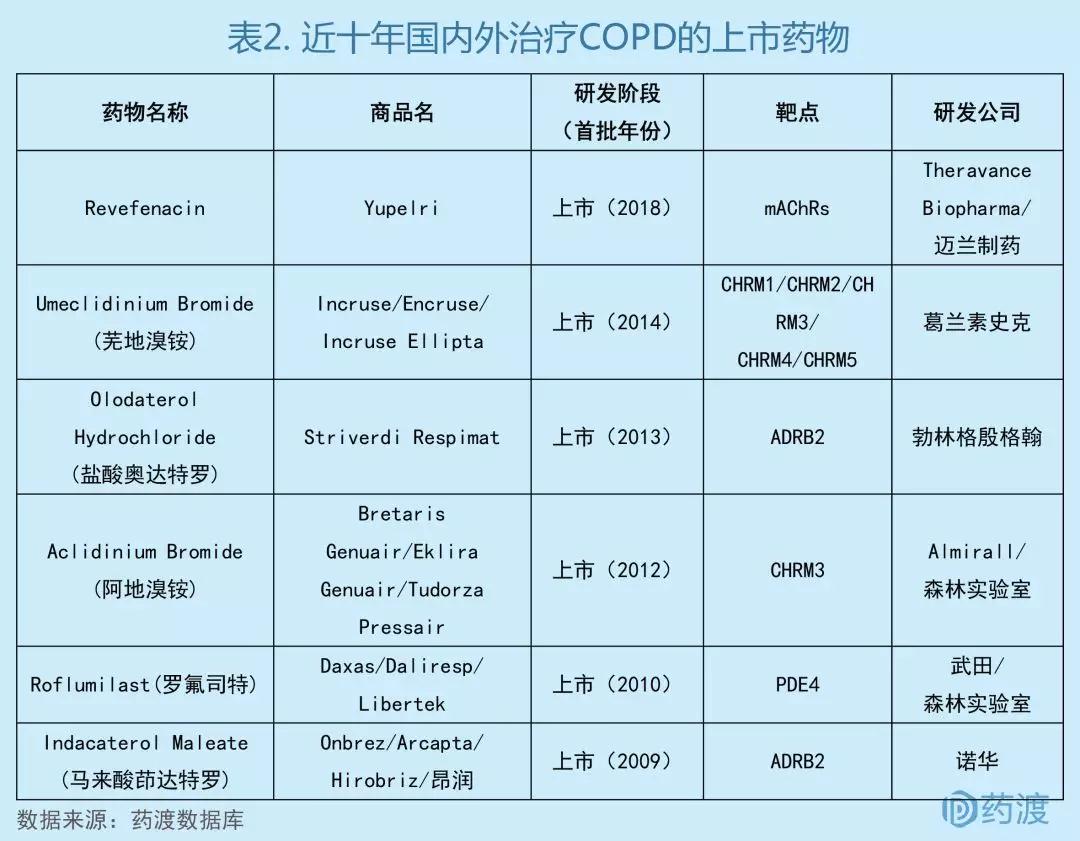
COPD是一种逐渐威胁生命的肺部疾病,会导致呼吸困难,且易恶化并引起严重疾病。该病的主要发病原因是接触烟草烟雾,其它风险因素包括接触室内和室外空气污染以及职业粉尘和烟雾。2016年全球有2.51亿例COPD病例,在许多国家,由于吸烟率较高和人口老龄化,慢性阻塞性肺病患者在未来几年还有可能增加;且COPD无法治愈,只能通过治疗缓解症状,提高生活质量并减少死亡风险[2]。
Revefenacin是一种长效毒蕈碱拮抗剂,通常被称为抗胆碱能药。它与毒蕈碱受体M1至M5的亚型具有相似的亲和力。在气道中,它通过抑制平滑肌上的M3受体导致支气管扩张而表现出药理作用,且吸入revefenacin后的作用主要表现在特定部位的支气管扩张[3]。
Revefenacin的获批是基于两项关键的重复性三期临床试验(NCT02459080和NCT02512510)。试验结果显示,通过比较1秒钟内的用力呼气量(FEV1)与给药12周后的FEV1相比,Revefenacin治疗组相较于安慰剂组的总体治疗效果方面具有显著的统计学意义(p = 0.025)和临床意义的改善(FEV1提升了100 mL)。Revefenacin治疗组中的不良事件(AEs)发生率与安慰剂组相当,严重不良事件(SAE)发生率较低。但是Revefenacin不能应用于急性恶化的COPD或治疗急性症状。此外,两家公司还完成了一项为期12个月的、开放标签的临床三期安全性试验研究,与噻托溴铵相比,Revefenacin治疗组没有发现新的安全问题,且该研究中的AE和SAE的发生率均较低,与噻托溴铵治疗组相似[4][5]。
Yupelri®目前是第一个也是唯一一个每日一次的雾化支气管扩张剂,使用十分方便,无疑会有很好的市场潜力,更重要的是它为患者和医生提供了一个更好的治疗选择。



